÷∏ æÑ© «ªØåW(xu®¶)‘áÑ©÷–µƒ“ªÓê°£‘⁄“ª∂®ΩÈŸ|(zh®¨)ólº˛œ¬£¨∆‰ÓÅ…´ƒÐ∞l(f®°)…˙◊ɪذ¢ƒÐÆa(ch®£n)…˙úÜù·ªÚ≥¡µÌ£¨“‘º∞”–ü…π‚¨F(xi®§n)œÛµ»°£≥£”√À¸ôzÚû»Ð“∫µƒÀ·âA–‘£ªµŒ∂®∑÷Œˆ÷–”√ÅÌ÷∏ 浌∂®ΩK¸c£ª≠h(hu®¢n)æ≥ôzúy÷–ôzÚû”–∫¶ŒÔ°£“ª∞„∑÷ûÈÀ·âA÷∏ æÑ©°¢—ıªØþÄ‘≠÷∏ æÑ©°¢ΩåŸ÷∏ æÑ©°¢Œ¸∏Ω÷∏ æÑ©µ»°£÷∏ æÑ©∑÷Óê 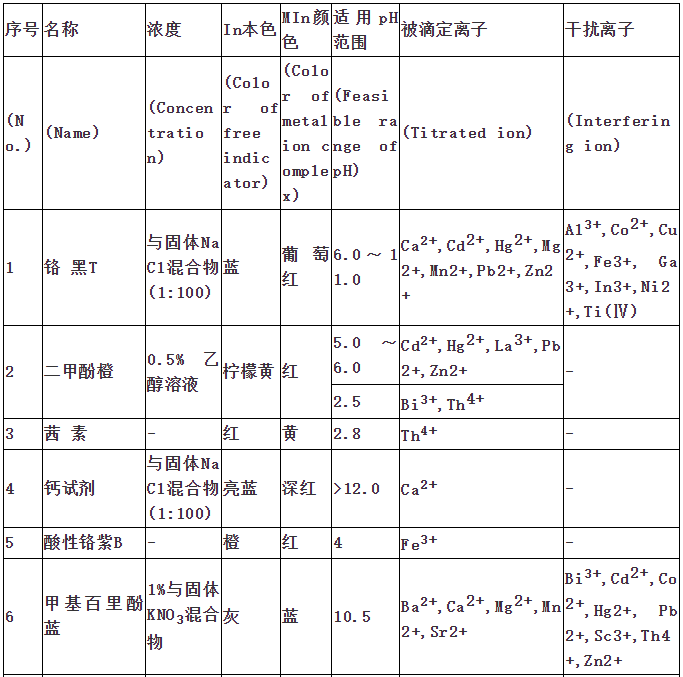
÷∏ æÑ©◊˜”√‘≠¿Ì ÷∏ æÑ©µƒ”√¡øÜñÓ}
1°¢À·âA÷∏ æÑ©
÷∏ æ»Ð“∫÷–H+ù‚∂»µƒ◊ɪأ¨ «“ª∑N”–ôC»ıÀ·ªÚ”–ôC»ıâA£¨∆‰À·–‘∫ÕâA–‘æþ”–≤ªÕ¨µƒÓÅ…´°£
“‘º◊ª˘≥»(Ka=10-3.4)ûÈ¿˝£¨»Ð“∫µƒpH<3.1ïr£¨≥ À·–‘£¨æþºt…´;ph>4.4ïr£¨≥ âA–‘£¨æþ¸S…´£ª∂¯‘⁄pH3.1~4.4£¨Ñt≥ˆ¨F(xi®§n)ºt¸SµƒªÏ∫œ…´≥»…´£¨∑Q÷ÆûÈ÷∏ æÑ©µƒ◊É…´∑∂á˙°£≤ªÕ¨µƒÀ·âA÷∏ æÑ©”–≤ªÕ¨µƒ◊É…´∑∂á˙°£
2°¢ªÏ∫œÀ·âA÷∏ æÑ©
◊¢£∫ªÏ∫œÀ·âA÷∏ æÑ©“™±£¥Ê‘⁄…Ó…´∆ø÷–°£
3°¢—ıªØþÄ‘≠÷∏ æÑ©
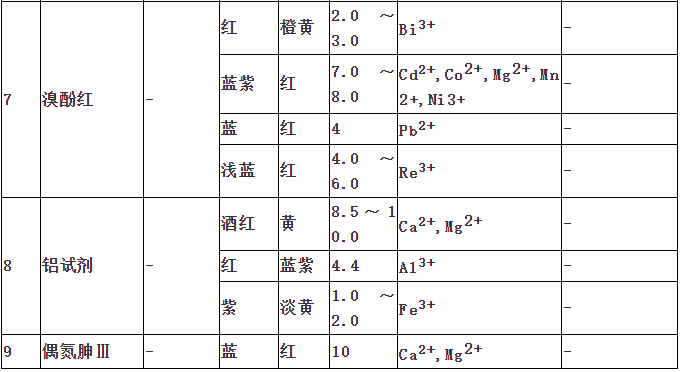
—ıªØþÄ‘≠÷∏ æÑ©”√”⁄—ıªØþÄ‘≠∑®»ð¡ø∑÷Œˆ°£œ¬±Ì¡–≥ˆ“ª–©‘⁄ΩÃåW(xu®¶)∫Õπ§◊˜÷–Ωõ(j®©ng)≥£ π”√µƒ≤ø∑÷—ıªØþÄ‘≠÷∏ æÑ©°£
4°¢Ωj(lu®∞)∫œ÷∏ æÑ©
‘⁄Ωj(lu®∞)∫œµŒ∂®÷–£¨Õ®≥£∂º «¿˚”√“ª∑NƒÐ≈cΩåŸÎx◊”…˙≥…”–…´≈‰∫œŒÔµƒÔ@…´Ñ©ÅÌ÷∏ 浌∂®þ^≥Ã÷–ΩåŸÎx◊”ù‚∂»µƒ◊ɪأ¨¥À∑NÔ@…´Ñ©∑QûÈΩåŸÎx◊”÷∏ æÑ©£¨º¥Ωj(lu®∞)∫œ÷∏ æÑ©°£
5°¢Œ¸∏Ω÷∏ æÑ©
Œ¸∏Ω÷∏ æѩ嶵Œ∂®ólº˛µƒ“™«Û£∫÷∏ æÑ©µƒŒ¸∏ΩƒÐ¡¶»ı”⁄¥˝úyÎx◊”°£
Œ¸∏Ω÷∏ æÑ© «“ªÓê”–ôC»æ¡œ£¨”√”⁄≥¡µÌ∑®µŒ∂®°£Æî(d®°ng)À¸±ªŒ¸∏Ω‘⁄ƒz¡£±Ì√Ê∫Û£¨ø…ƒÐ «”…”⁄–Œ≥…¡Àƒ≥∑NªØ∫œŒÔ∂¯åß(d®£o)÷¬÷∏ æÑ©∑÷◊”ΩY(ji®¶)òã(g®∞u)µƒ◊ɪأ¨èƒ∂¯“˝∆ÓÅ…´µƒ◊ɪذ£‘⁄≥¡µÌµŒ∂®÷–£¨ø…“‘¿˚”√À¸µƒ¥À∑N–‘Ÿ|(zh®¨)ÅÌ÷∏ 浌∂®µƒΩK¸c°£
Œ¸∏Ω÷∏ æÑ©ø…∑÷ûÈÉ…¥ÛÓê£∫“ªÓê «À·–‘»æ¡œ£¨»Áü…π‚¸Sº∞∆‰—Ð…˙ŒÔ£¨À¸ÇÉ «”–ôC»ıÀ·£¨ƒÐΩ‚Îx≥ˆ÷∏ æÑ©ÍéÎx◊”£ª¡Ì“ªÓê «âA–‘»æ¡œ£¨»Áº◊ª˘◊œµ»£¨À¸ÇÉ «”–ôC»ıâA£¨ƒÐΩ‚Îx≥ˆ÷∏ æÑ©ÍñÎx◊”°£
6°¢ü…π‚÷∏ æÑ©
µŒ∂®∫Õ¥_∂®úÜù·“∫Ûw∫Õ”–…´“∫ÛwµƒpHø…“‘ π”√ü…π‚÷∏ æÑ©°£‘⁄µŒ∂®þ^≥Ã÷–ü…π‚…´◊É≤ª Г∫ÛwÓÅ…´∫Õ∆‰Õ∏√˜∂»µƒ”∞Ì루“Ú¥À≥£±ªþx”√°£
‘⁄åçÎHπ§◊˜÷–£¨»‚—€ «Îy“‘ú (zh®≥n)¥_µÿ”^≤Ï≥ˆ÷∏ æÑ©◊É…´¸cÓÅ…´µƒŒ¢–°µƒ∏ƒ◊É°£»ÀÇɃøúyÀ·âA÷∏ æѩ胓ª∑NÓÅ…´◊É?y®≠u)È¡Ì“ª∑NÓÅ…´µƒþ^≥ã¨÷ªƒÐ‘⁄“ª∂®µƒpH◊ɪØ∑∂á˙É»(n®®i)≤≈ƒÐ∞l(f®°)…˙£¨º¥÷ª”–Æî(d®°ng)“ª∑NÓÅ…´œýÆî(d®°ng)”⁄¡Ì“ª∑NÓÅ…´ù‚∂»µƒ Ʊ∂ïr≤≈ƒÐ√„èä±Ê’J(r®®n)∆‰ÓÅ…´µƒ◊ɪذ£‘⁄þ@∑NÓÅ…´◊ɪصƒÕ¨ïr£¨ΩÈŸ|(zh®¨)ö‰úÁæ˙…˙ŒÔ÷∏ æÑ©µƒpH÷µÑt”…“ªÇÄ÷µ◊ÉµΩ¡Ì“ªÇÄ÷µ°£
»Ð“∫µƒÓÅ…´◊ɪØ∑∂á˙∑QûÈ÷∏ æÑ©µƒ◊É…´∑∂á˙º¥◊É…´”Ú°£‘⁄◊É…´∑∂á˙É»(n®®i)£¨Æî(d®°ng)»Ð“∫µƒpH÷µ∏ƒ◊Éïr£¨âA…´≥…∑÷∫ÕÀ·…´≥…∑÷µƒ±»÷µÎS÷Æ∏ƒ◊É£¨÷∏ æÑ©µƒÓÅ…´“≤∞l(f®°)…˙∏ƒ◊É°£÷∏ æÑ©µƒ◊É…´∑∂á˙ºs2ÇÄpHÜŒŒª°£”…”⁄»Àµƒ“ï”Xå¶∏˜∑NÓÅ…´µƒ√Ù∏–≥Ã∂»≤ªÕ¨£¨º”…œ‘⁄◊É…´”ÚÉ»(n®®i)÷∏ æÑ©≥ ¨F(xi®§n)ªÏ∫œ…´£¨É…∑NÓÅ…´ª•œý”∞Ìë”^≤Ï£¨À˘“‘åçÎH”^≤ÏΩY(ji®¶)π˚≈c¿Ì’ì÷µ”–≤ÓÑe£¨¥Û∂ýîµ(sh®¥)÷∏ æÑ©µƒ◊É…´∑∂á˙–°”⁄2ÇÄpHÜŒŒª°£
Îp…´÷∏ æÑ©µƒ◊É…´∑∂á˙≤ª Ð∆‰”√¡øµƒ”∞Ì루µ´“Ú÷∏ æÑ©±æ…ÌæÕ «À·ªÚâA£¨÷∏ æÑ©µƒ◊É…´“™œ˚∫ƒ“ª∂®µƒµŒ∂®Ñ©£¨èƒ∂¯‘ˆ¥Ûúy∂®µƒ’`≤Ó°£å¶”⁄ÜŒ…´÷∏ æÑ©∂¯—‘£¨”√¡øþ^∂ý£¨ï˛ π”√◊É…´∑∂á˙œÚpH÷µúp–°µƒ∑ΩœÚ∞l(f®°)…˙“∆Ñ”£¨“≤ï˛‘ˆ¥ÛµŒ∂®µƒ’`≤Ó°£¿˝»Á:”√0.1mol/LNaOHµŒ∂®0.1mol/LHAc£¨pHsp=8.5,ÕªÐS∑∂á˙ûÈpH8.70-9.00£¨µŒ∂®Ûw∑e»ÙûÈ50mL£¨µŒ»Î2~3µŒ∑”Ù£¨¥Ûºs‘⁄pH=9ïr≥ˆ¨F(xi®§n)ºt…´£ª»ÙµŒ»Î10~15µŒ∑”Ù£¨Ñt‘⁄pH=8ïr≥ˆ¨F(xi®§n)ºt…´°£Ô@»ª∫Û’þµƒµŒ∂®’`≤Ó“™¥Ûµ√∂ý°£
÷∏ æÑ©”√¡øþ^∂ý£¨þÄï˛”∞Ìë◊É…´µƒ√Ù‰J–‘°£¿˝»Á£∫“‘º◊ª˘≥»ûÈ÷∏ æÑ©£¨”√HClµŒ∂®NaOH»Ð“∫£¨ΩK¸cûÈ≥»…´£¨»Ùº◊ª˘≥»”√¡øþ^∂ýÑtΩK¸c√Ù‰J–‘æÕð^≤Ó°£
≥£”√÷∏ æÑ©µƒ≈‰÷∆£®π©Ö¢øº£©
(æþÛw≈‰÷∆∑Ω∑®“‘åçÚûòÀ(bi®°o)ú (zh®≥n)ûÈú (zh®≥n))
1°¢∂˛±Ω∞∑ª«À·‚c÷∏ æ“∫£∫
2°¢∂˛±ΩŸ…ά÷∏ æ“∫£∫
»°∂˛±ΩŸ…ά1g£¨º”““¥º100mL π»ÐΩ‚£¨º¥µ√°£
»°Îp¡ÚÎÍ50mg£¨º”““¥º100mL π»ÐΩ‚£¨º¥µ√°£
4°¢ Ø»Ô÷∏ æ“∫£∫
»° Ø»Ô∑€ƒ©10g,º”““¥º40mL£¨ªÿ¡˜÷Û∑–1–°ïr,Ïo÷√£¨ÉA»•…œå”«Â“∫£¨‘Ÿ”√Õ¨“ª∑Ω∑®Ãé¿Ì∂˛¥Œ£¨√ø¥Œ”√““¥º30mL£¨öà‘¸”√ÀÆ10mLœ¥úÏ£¨ÉA»•œ¥“∫£¨‘Ÿº”ÀÆ50mL£¨÷Û∑–£¨∑≈¿‰£¨ûVþ^£¨º¥µ√°£◊É…´∑∂á˙pH4.5~8.0(ºt°˙À{(l®¢n))°£
5°¢º◊∑”ºt÷∏ æ“∫£∫
»°º◊∑”ºt0.1g£¨º”0.05mol/Lö‰—ıªØ‚c»Ð“∫5.3ml π»ÐΩ‚£¨‘Ÿº”ÀÆœ°·å÷¡100mL£¨º¥µ√°£◊É…´∑∂á˙ pH7.2~8.8(¸S°˙ºt)
6°¢º◊∑”ºt-˜Íœ„≤ð∑”À{(l®¢n)ªÏ∫œ÷∏ æ“∫£∫
»°º◊∑”ºt÷∏ æ“∫1∑ð≈c0.1%˜Íœ„≤ð∑”À{(l®¢n)»Ð“∫3∑ð,ªÏ∫œ£¨º¥µ√°£
º◊ª˘ºt÷∏ æ“∫»°º◊ª˘ºt0.1g£¨º”0.05mol/Lö‰—ıªØ‚c»Ð“∫7.4mL π»ÐΩ‚£¨‘Ÿº”ÀÆœ°·å÷¡200mL£¨º¥µ√°£◊É…´∑∂á˙ pH4.2~6.3(ºt°˙¸S)°£
7°¢1g/L(0.1%) º◊ª˘ºt÷∏ æÑ©µƒ≈‰÷∆∑Ω∑®
À˘–ËÀé∆∑£∫º◊ª˘ºt°£
”√Õæ£∫≈‰÷∆º◊ª˘ºt-‰Âº◊∑”æGªÏ∫œ÷∏ æÑ©°£
≈‰÷∆∑Ω∑®£∫∑Q»°1gº◊ª˘ºt£¨”√1000mLüoÀÆ““¥º»ÐΩ‚°£
8°¢º◊ª˘ºt-Åܺ◊À{(l®¢n)ªÏ∫œ÷∏ æ“∫£∫
»°0.1%º◊ª˘ºtµƒ““¥º»Ð“∫20mL£¨º”0.2%Åܺ◊À{(l®¢n)»Ð“∫8mL£¨ìuÑÚ£¨º¥µ√°£
9°¢º◊ª˘ºt-‰Âº◊∑”æGªÏ∫œ÷∏ æ“∫£∫
»°0.1%º◊ª˘ºtµƒ““¥º»Ð“∫20mL£¨º”0.2%‰Âº◊∑”æGµƒ““¥º»Ð“∫30mL£¨ìuÑÚ£¨º¥µ√°£
10°¢0.1%(1g/L)º◊ª˘≥»÷∏ æ“∫£∫
»°º◊ª˘≥»0.1g£¨º”ÀÆ100mL π»ÐΩ‚£¨ü·»ÐΩ‚£¨¿‰Ös∫Ûþ^ûVlj”√°£◊É…´∑∂á˙ pH3.2~4.4(ºt°˙¸S)°£
’f√˜£∫√ø100 mLµŒ∂®“∫º”1µŒ°£º”µƒ¡øô∂ý£¨∑¥∂¯≤ª√˜¥_°£±æ÷∏ æ“∫þm”√”⁄»ıâAªÚ∞±°¢ö‰—ıªØ‚}°¢ö‰—ıªØÊJ°¢ö‰—ıªØ‰^°¢ö‰—ıªØÊVµƒµŒ∂®£¨≤ªþm”√”⁄»ıÀ·£¨¿˝»Áö‰«ËÀ·°¢ÃºÀ·°¢ÅÜ…ÈÀ·°¢≈À·°¢„tÀ·°¢”–ôCÀ·µƒµŒ∂®£¨“Ú¥ÀµŒ∂®èäÀ·ïr£¨þ@–©À·π≤¥Ê «õ]”–”∞Ì뵃°£œıÀ·ƒÐ∆∆⃺◊ª˘≥»£¨π ≤ªþm”√£¨µ´ø…º”»Îþ^¡øµƒâA‘ŸþM(j®¨n)––µŒ∂®°£º◊ª˘≥»“≤”√”⁄““¥º»Ð“∫µƒµŒ∂®°£
11°¢º◊ª˘≥»-∂˛º◊±ΩÀ{(l®¢n)FFªÏ∫œ÷∏ æ“∫£∫
»°º◊ª˘≥»≈c∂˛º◊±ΩÀ{(l®¢n)FF∏˜0.1g£¨º”““¥º100mL π»ÐΩ‚£¨º¥µ√°£
12°¢ýè∂˛µ™∑∆÷∏ æ“∫£∫
»°¡ÚÀ·ÅÜËF0.5g£¨º”ÀÆ100mL π»ÐΩ‚,º”¡ÚÀ·2µŒ≈cýè∂˛µ™∑∆0.5g,ìuÑÚ£¨º¥µ√°£±æ“∫ë™(y®©ng)≈R”√–¬÷∆°£
13°¢ÐÁÀÿª«À·‚c÷∏ æ“∫£∫
»°ÐÁÀÿª«À·‚c0.1g£¨º”ÀÆ100mL π»ÐΩ‚£¨º¥µ√°£◊É…´∑∂á˙ pH3.7~5.2(¸S°˙◊œ)
14°¢ü…π‚¸S÷∏ æ“∫£∫
»°ü…π‚¸S0.1g£¨º”““¥º100mL π»ÐΩ‚£¨º¥µ√°£
15°¢‚}¸SæGÀÿ÷∏ æÑ©£∫
»°‚}¸SæGÀÿ0.1g£¨º”¬»ªØ‚õ10g£¨—–ƒ•æ˘ÑÚ£¨º¥µ√°£
16°¢‚}◊œºtÀÿ÷∏ æÑ©£∫
»°‚}◊œºtÀÿ0.1g£¨º”üoÀÆ¡ÚÀ·‚c10g,—–ƒ•æ˘ÑÚ£¨º¥µ√°£
17°¢Ω™¸S÷∏ æ“∫£∫
»°Ω™¸S∑€ƒ©20g£¨”√¿‰ÀÆΩ˛ùn4¥Œ£¨√ø¥Œ100mL,≥˝»•ÀƻЖ‘ŒÔŸ|(zh®¨)∫Û£¨öà‘¸‘⁄100°Ê∏…‘Ô£¨º”““¥º100mL£¨Ω˛ùnîµ(sh®¥)»’£¨ûVþ^£¨º¥µ√°£
18°¢ΩY(ji®¶)æß◊œ÷∏ æ“∫£∫
»°ΩY(ji®¶)æß◊œ0.5g£¨º”±˘¥◊À·100mL π»ÐΩ‚£¨º¥µ√°£
19°¢∑”Ù÷∏ æ“∫£∫
0.1%£®1g/L£©∑”Ù÷∏ æÑ©µƒ≈‰÷∆∑Ω∑®
0.1% µƒ∑”Ù÷∏ æÑ© «÷∏100mL»Ð“∫ π”√ 0.1g µƒ∑”Ù°£
≈‰÷√∑Ω∑®£∫∑Q¡ø 0.1g ∑”Ù£¨»ª∫Û”√…Ÿ¡ø95%““¥ºªÚ’þüoÀÆ““¥º»ÐΩ‚£¨∂®¡øÞD(zhu®£n)“∆÷¡100mL»ð¡ø∆ø∫Û‘Ÿ”√““¥º∂®»ðœ°·åµΩ100mLº¥ø…°£
0.5%£®5g/L£©∑”Ù÷∏ æÑ©µƒ≈‰÷∆∑Ω∑®
»° 0.5g ∑”Ù£¨»Ð”⁄““¥º£¨”√““¥ºœ°·å÷¡ 100mL£¨üo–˺”ÀÆ°£◊É…´∑∂á˙ pH8.3°´10.0£®üo…´°˙ºt£©°£
’f√˜£∫±æ÷∏ æ“∫å¶À·√Ù∏–£¨¿˝»Á£¨å¶ÃºÀ·◊É…´£¨ø…”√ÅÌôz≤È «∑Ò∫¨ÃºÀ·ö‚°£þm”√”⁄èäâAµŒ∂®üoôCÀ·°¢”–ôC»ıÀ·£¨“≤þm”√”⁄““¥º»Ð“∫µƒµŒ∂®°£èäÀ·µŒ∂®»ıâA(¿˝»Á∞±)≤ªþm∫œ°£πËÀ·∫Õ‰X¥Ê‘⁄£¨å¶±æ»Ð“∫◊É…´üo∑¡µK°£≈cù‚âAΩ””|ºt…´œ˚ ß°£
20°¢„t∫⁄T÷∏ æÑ©(5g/L)µƒ≈‰÷∆∑Ω∑®
∑Q»°0.50g„t∫⁄T∫Õ4.5g¬»ªØ¡u∞∑£¨»Ð”⁄““¥º÷–£¨”√““¥ºœ°·å÷¡100mL£¨ŸA¥Ê”⁄◊ÿ…´∆ø÷–°£ø…±£≥÷?j®´n)?sh®¥)‘¬≤ª◊ÉŸ|(zh®¨)°£
21°¢5g /LµÌ∑€÷∏ æ“∫£∫
»°ø…»Ð–‘µÌ∑€0.5g£¨º”ÀÆ5mLîáÑÚ∫Û£¨æèæèÉA»Î100mL∑–ÀÆ÷–£¨ÎSº”ÎSîá∞Ë£¨¿^¿m(x®¥)÷Û∑–2∑÷Á䣨∑≈¿‰£¨ÉA»°…œå”«Â“∫£¨º¥µ√°£±æ“∫ë™(y®©ng)≈R”√–¬÷∆°£
22°¢µ‚ªØ‚õµÌ∑€÷∏ æÑ©µƒ≈‰÷∆∑Ω∑®
»°µ‚ªØ‚õ 0.2g £¨º”–¬÷∆µƒµÌ∑€÷∏ æ“∫100mL π»ÐΩ‚°£
23°¢¡ÚÀ·ËF‰@÷∏ æ“∫£∫
»°¡ÚÀ·ËF‰@8g£¨º”ÀÆ100mL π»ÐΩ‚£¨º¥µ√°£
24°¢‰Â∑”À{(l®¢n)÷∏ æ“∫£∫
»°‰Â∑”À{(l®¢n)0.1g£¨º”0.05mol/Lö‰—ıªØ‚c»Ð“∫3.0mL π»ÐΩ‚£¨‘Ÿº”ÀÆœ°·å÷¡200mL£¨º¥µ√°£◊É…´∑∂á˙ pH2.8~4.6(¸S°˙À{(l®¢n)æG)°£
25°¢‰Â˜Íœ„≤ð∑”À{(l®¢n)÷∏ æ“∫£∫
»°‰Â˜Íœ„≤ð∑”À{(l®¢n)0.1g£¨º”0.05mol/Lö‰—ıªØ‚c»Ð“∫3.2mL π»ÐΩ‚£¨‘Ÿº”ÀÆœ°·å÷¡200mL£¨º¥µ√°£◊É…´∑∂á˙ pH6.0~7.6(¸S°˙À{(l®¢n))°£
26°¢˜Íœ„≤ð∑”Ù÷∏ æ“∫£∫
»°˜Íœ„≤ð∑”À{(l®¢n)0.1g£¨º”0.05mol/Lö‰—ıªØ‚c»Ð“∫4.3mL π»ÐΩ‚£¨‘Ÿº”ÀÆœ°·å÷¡200mL£¨º¥µ√°£◊É…´∑∂á˙ pH1.2~2.8(ºt°˙¸S)£ªpH8.0~9.6(¸S°˙◊œÀ{(l®¢n))°£
»°˜Íœ„≤ð∑”Ù0.1g£¨º”““¥º100mL π»ÐΩ‚£¨º¥µ√°£◊É…´∑∂á˙ pH9.3~10.5(üo…´°˙À{(l®¢n))°£
27°¢˜Íœ„≤ð∑”À{(l®¢n)÷∏ æ“∫£∫
 ÷ôC∞Ê
÷ôC∞Ê





